猪精液外泌体变身眼药水:靶向治疗视网膜母细胞瘤的新路径
视网膜母细胞瘤(Retinoblastoma, RB)是儿童最常见的眼内恶性肿瘤,传统治疗依赖静脉化疗、眼部注射甚至眼球摘除,创伤大、风险高。如何用非侵入性方式把药物精准送达眼底,一直是眼科药递领域的难题。
最近的一项研究提供了一种出人意料的解法:从猪精液中提取外泌体(SEVs),改造后制成眼药水,用于靶向治疗视网膜母细胞瘤。
为什么选精液外泌体?
外泌体(Exosomes)是细胞分泌的纳米级囊泡,天然具备良好的生物相容性和跨膜运输能力,近年来被视为理想的药物递送载体。但普通外泌体很难穿透眼部的多重屏障(角膜上皮、结膜等紧密连接)。
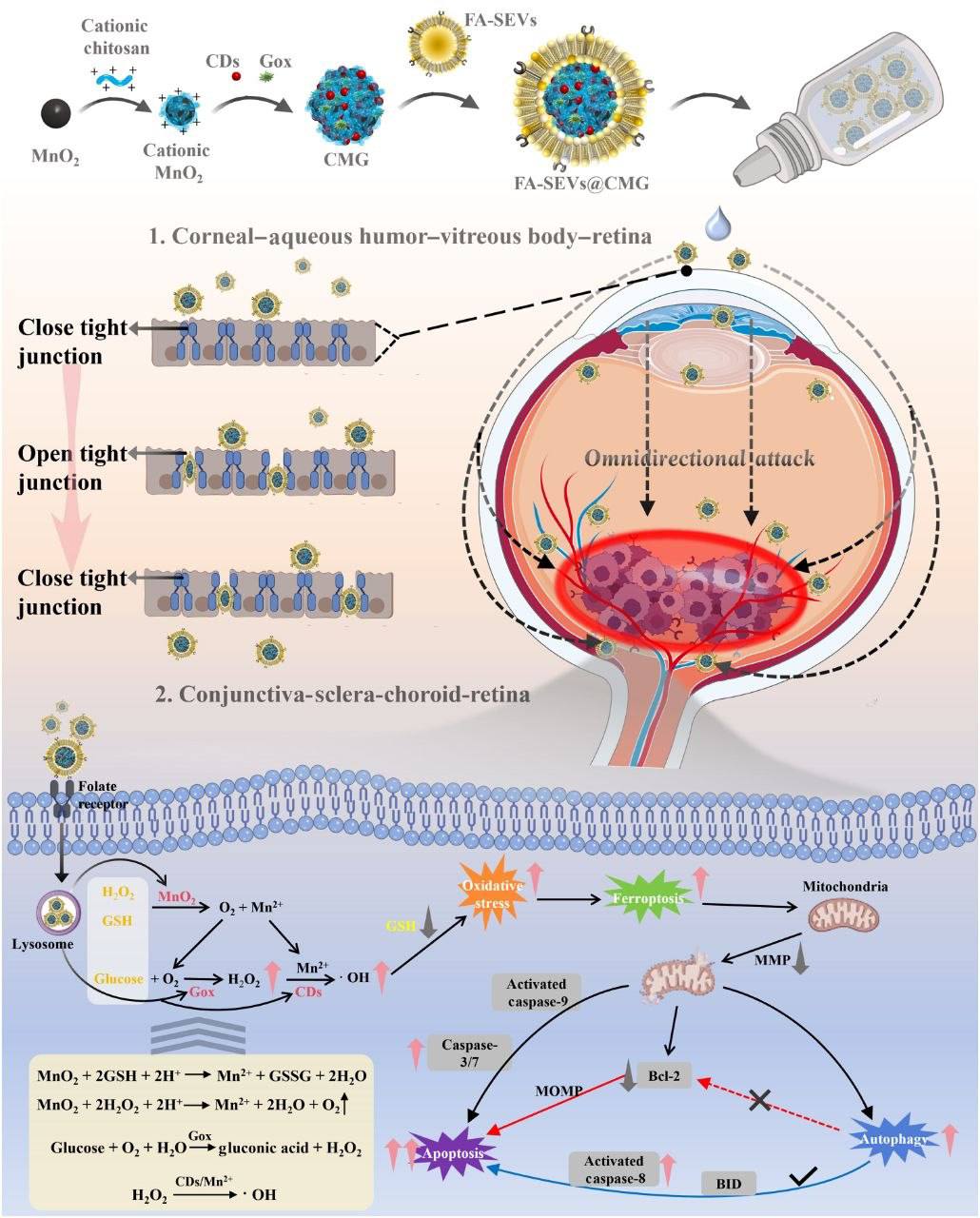
精液来源的外泌体(Semen-derived Extracellular Vesicles, SEVs)在这一点上表现出独特优势。研究发现,SEVs 表面天然携带表皮生长因子(EGF),EGF 能够暂时打开角膜和结膜上皮细胞间的紧密连接(tight junctions),为药物打开一条"临时通道"。
换句话说,SEVs 本身就是一把自带"钥匙"的纳米载体——它能自己开门进入眼部深层组织。
双重改造:靶向 + 杀伤
研究团队在 SEVs 的基础上进行了两步功能化改造:
靶向增强:在 SEVs 表面接枝叶酸(Folic Acid, FA)。叶酸受体在多种肿瘤细胞表面高表达,接上叶酸后,SEVs 就像装了导航系统,能主动识别并结合视网膜母细胞瘤细胞。
杀伤载荷:在 SEVs 内部装载一种纳米酶系统(CMG)。这种纳米酶到达肿瘤微环境后,能催化产生活性氧(ROS),触发肿瘤细胞凋亡(程序性死亡)。
改造后的 SEVs-FA/CMG 以眼药水形式滴入眼表,经角膜和结膜屏障渗透后,精准到达眼底肿瘤部位,定向释放杀伤载荷。
动物实验结果
在视网膜母细胞瘤动物模型中,SEVs-FA/CMG 滴眼液展现出了明确的抗肿瘤效果:
- 肿瘤生长受到显著抑制
- 递送效率高于对照组外泌体
- 未观察到明显的眼表毒性或系统性副作用
与传统的玻璃体腔注射相比,滴眼给药的侵入性大幅降低,患者(尤其是儿童患者)的依从性也会显著提高。
局限与展望
这项研究的核心贡献在于证明了精液外泌体作为眼部药物递送载体的可行性,但距离临床应用仍有距离:
- 目前仅在动物模型中验证,人体试验尚未开展
- SEVs 的长期生物安全性需要更系统的评估
- 大规模制备和质量控制也是产业化必须解决的问题
不过,这条思路的价值在于:它拓展了外泌体递送系统的来源选择,也为非侵入性眼病治疗提供了一个值得继续探索的方向。
- 人类脂肪组织血管细胞图谱:肥胖时内皮细胞出现7种亚型5/2/2026
- 男性避孕重大突破:靶向减数分裂实现安全可逆的非激素方案4/8/2026
- 羊毛角蛋白膜修复骨缺损:首次活体验证完成5/2/2026
- 50 位科学家发布五步计划,应对耐药真菌全球威胁4/15/2026