激素敏感性脂肪酶的核内新身份与肥胖研究
如果你翻开任何一本生物化学教材,关于脂肪分解的章节大概都长一个样:激素敏感性脂肪酶(HSL)驻扎在脂肪滴表面,收到肾上腺素信号后激活,把甘油三酯拆成脂肪酸供身体使用。这套叙事从 1960 年代起几乎没变过。
但 2025 年 10 月发表在 Cell Metabolism 上的一项研究,给这位「老熟人」补上了一个完全不同的身份——HSL 不只是脂肪滴上的「剪刀」,它还会走进细胞核,参与基因调控,维持脂肪组织的健康状态。
反直觉的缺失表型
按照经典逻辑,如果 HSL 是分解脂肪的关键酶,敲除它应该导致脂肪堆积、小鼠变胖。但实际情况恰恰相反:HSL 缺失的小鼠和人类患者都出现了「脂肪营养不良」(lipodystrophy)——脂肪组织不是变多了,而是变少了。
这个矛盾提示研究者:HSL 的功能远不止分解脂肪那么简单。
细胞核里的意外发现
研究团队发现,HSL 大量存在于脂肪细胞的细胞核中,并且与染色质结合。在小鼠模型中,只有保留核内 HSL 表达的个体才能维持正常的脂肪组织;而仅保留细胞质中 HSL 酶活性的个体,仍然会出现脂肪营养不良。
这意味着核内的 HSL 扮演着不可替代的角色。基因沉默实验显示,HSL 能独立于其酶活性,对线粒体氧化磷酸化和细胞外基质基因产生相反方向的调控——前者上调,后者下调。这些通路共同维持脂肪细胞的健康。
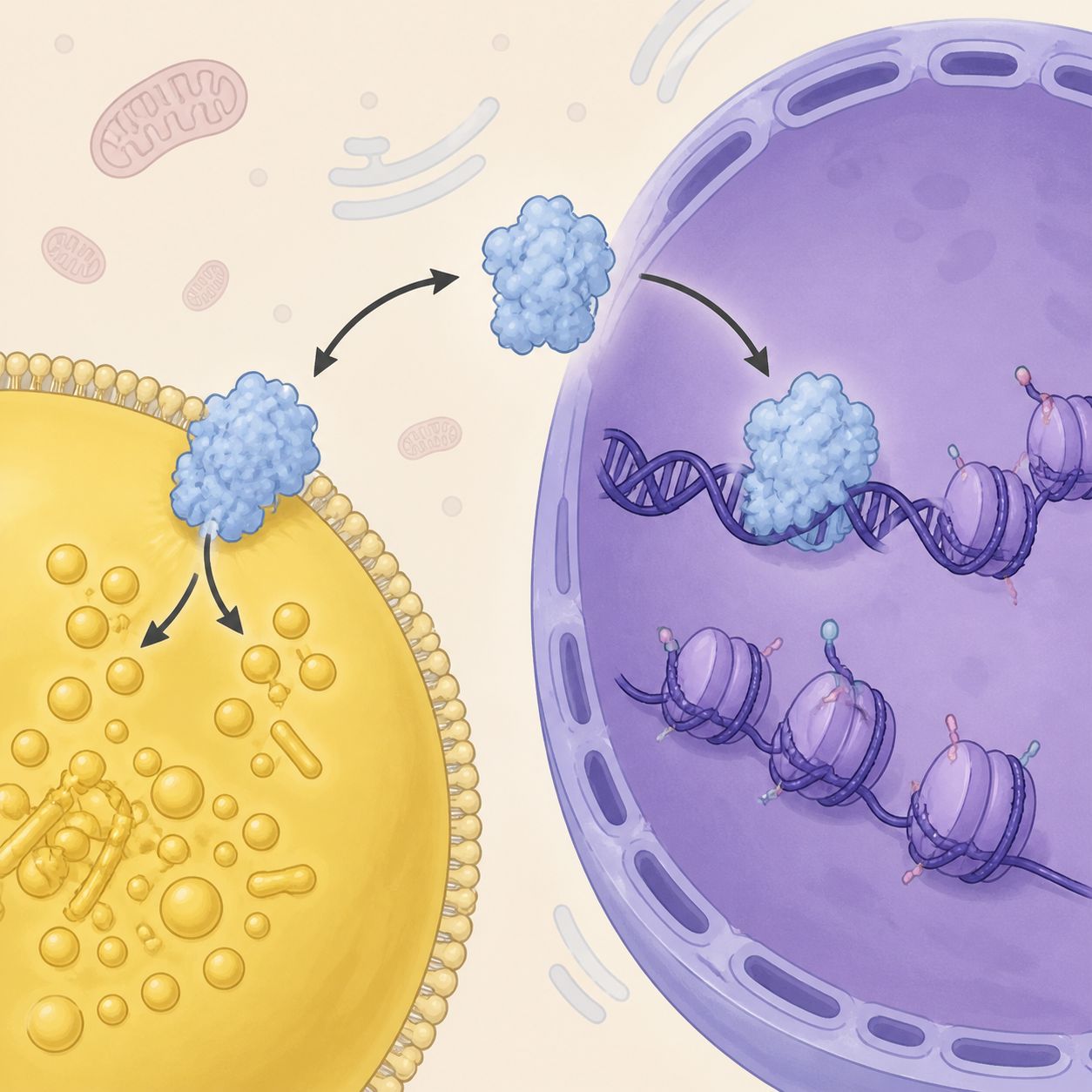
SMAD3 介导的核质穿梭
机制层面,HSL 通过与 TGF-β 信号通路中的 SMAD3 蛋白相互作用进入细胞核。而 PKA 介导的磷酸化则会触发 HSL 的核输出——这正是禁食状态下发生的事情。肾上腺素激活 PKA,HSL 被磷酸化后离开细胞核,回到脂肪滴表面执行经典的脂肪分解任务。
在高脂饮食条件下,情况反过来了:HSL 更多地滞留在核内。这种动态的核质穿梭,让 HSL 能根据营养状态在两个角色之间切换。
重新理解肥胖
这项研究带来的核心启发是:肥胖的本质可能不在于「脂肪太多」,而在于脂肪细胞功能是否正常。HSL 缺失导致的脂肪营养不良与肥胖看似两个极端,但都意味着脂肪组织无法正常运作,都会引发代谢和心血管并发症。
以下几点值得关注:
- 脂肪组织的健康与否可能比脂肪量的多少更重要
- HSL 的核内功能为理解脂肪营养不良的发病机制提供了新线索
- 未来或可通过调控 HSL 的亚细胞定位来影响脂肪组织状态
需要强调的是,这是一项基础研究,距离临床应用还有很长的路。它的价值在于修正了学界对 HSL 的单一认知,为肥胖和相关代谢疾病的理解打开了新的视角。
来源:Dufau J, et al. Nuclear hormone-sensitive lipase regulates adipose tissue mass and adipocyte metabolism. Cell Metabolism, 2025. DOI: 10.1016/j.cmet.2025.09.014
- 线粒体的“串珠”机制:一个被忽视了一百年的 DNA 分布密码4/28/2026