多族群研究揭示近视新基因,预测模型或助早期干预
近视是全球最常见的视力问题,影响超过一半人口,严重时可导致视力模糊甚至失明。长期以来,科学家一直在探索近视背后的遗传机制,但大多数研究集中在欧洲人群,对其他族群的覆盖严重不足。
4 月 20 日发表在 Nature Genetics 上的一项研究改变了这一局面。由 Fei-Fei Cheng、Jian Yang 等人组成的国际团队,对欧洲(149.5 万人)、东亚(12.1 万人)和非洲(14.5 万人)三大族群的基因组数据进行了分层和跨族群 meta 分析,这是迄今为止规模最大的屈光不正多族群基因组关联研究。
241 个新发现的遗传变异
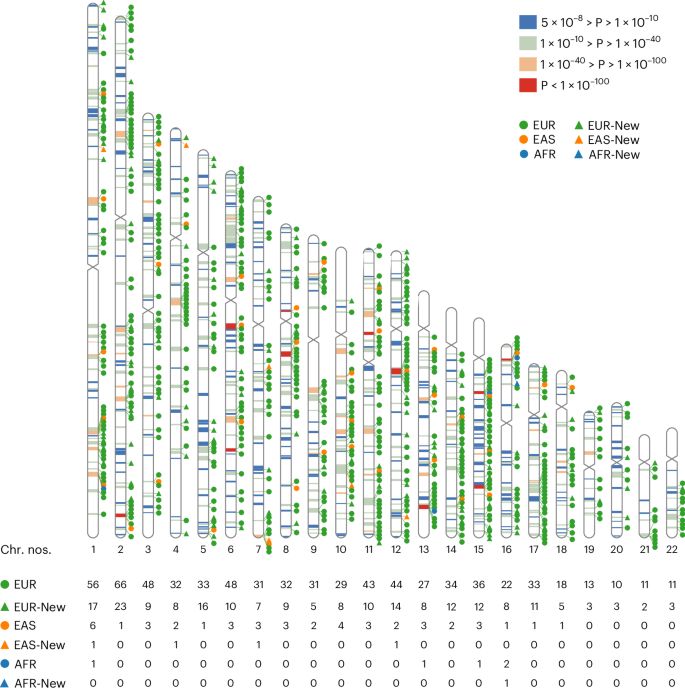
跨族群 meta 分析共识别出 932 个与屈光不正相关的变异体,其中 241 个是此前从未被报道的。通过统计精细定位,研究团队锁定了 16 个高置信的潜在因果变异体,基因优先级分析则标记出 23 个与眼发育直接相关的基因。
在新发现的变异中,有 4 个为东亚人群特有,1 个为非洲人群特有。这表明不同族群的近视遗传基础存在真实的生物学差异,单一族群数据构建的遗传模型在其他族群中的预测能力会打折扣。
多基因预测的临床潜力
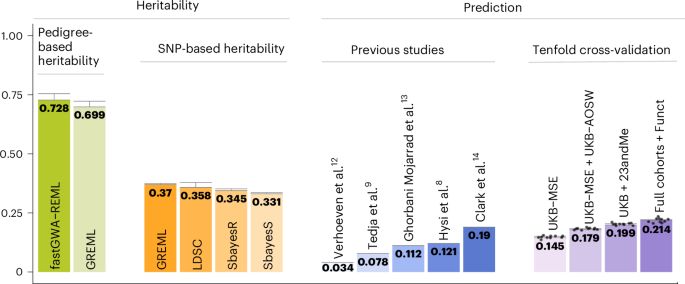
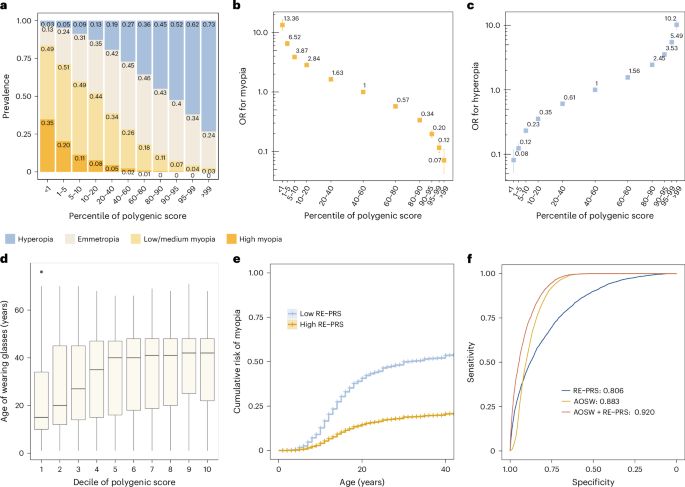
研究的另一项核心成果是构建了一个增强型多基因预测模型。该模型整合了功能注释信息,能解释屈光不正 21.4% 的表型变异,预测高风险近视的 AUC(受试者工作特征曲线下面积)达到 0.806。
这个模型的特别之处在于,它不仅能识别高风险人群,还能区分近视的起始阶段、进展速度和严重程度——临床医生可以根据这些分层信息制定差异化的干预策略。
仍需跨越的障碍
尽管结果令人鼓舞,但距离临床应用仍有明显差距。非洲样本量(14.5 万)远低于欧洲(149.5 万),这种不均衡可能导致模型在非欧洲族群上的预测精度被高估。研究团队也指出,需要更大规模的外部队列来验证模型的泛化能力。
此外,多基因预测模型解释了 21.4% 的变异,意味着大部分屈光不正的遗传因素仍未被捕获。环境因素(如户外活动时间、近距离用眼习惯)与遗传因素的交互作用,也需要在未来的研究中进一步厘清。
来源:Nature Genetics · Cheng et al. (2026) · DOI
- 研究称精子储存时间越长质量越差,更频繁射精或有助受孕3/26/2026
- 终生认知丰富度与阿尔茨海默病:Rush 大学近 2000 人研究显示晚 5 年发病4/29/2026
- 超加工食品或与大腿肌肉脂肪浸润有关,MRI 研究揭示潜在关联4/29/2026
- 几种植物成分组合,抗炎效果翻数百倍:新研究揭示协同机制4/24/2026
- 睡前 3 小时不吃:一项 RCT 如何证明禁食与睡眠对齐能改善心血管健康4/25/2026
- 孤独感影响老年记忆?研究揭示关键差异4/26/2026
- 小麦面粉或助长体重?小鼠实验揭示其代谢奥秘4/26/2026
- 每周吃几次鸡蛋,阿尔茨海默病风险更低?5/15/2026
- SP8 基因被发现参与肢体再生,小鼠实验验证部分修复效果4/20/2026
- 每天喝咖啡,真的只是提神吗?研究发现它在悄悄影响肠道和情绪5/13/2026
- 蝴蝶拟态的遗传密码:跨越1.2亿年的进化可预测性5/12/2026
- 蚊子为什么总偏爱某些人?不是血型,是皮肤气味5/17/2026
- 每周一次HIIT也能减脂?Nature子刊315人试验结果5/24/2026
- Nature: 睡眠时长与生物衰老的U型关系5/17/2026
- 每天8500步:减重靠吃,防反弹靠走5/25/2026
- 每周运动150分钟够了吗?新研究给出更精确的答案5/26/2026